ビタミンCの還元型と酸化型とは?
まず,酸化と還元の説明をします.金属が「さびる」のが酸化の代表例ですが,金属が酸素と結合することです.後で出てきますが,水素や電子を奪われることも酸化です.その逆の反応が還元です.例えば,酸化された金属である「さび」から酸素を取り除いて元の金属に戻す反応です.
鉄の精錬を考えます.鉄鉱石の主成分は鉄(元素記号Fe)が酸素と結合した酸化鉄Fe2O3です.炭素の塊であるコークスから一酸化炭素(CO)を発生させて反応させ,下記のように酸化鉄から酸素を取り除いて金属の鉄を生成します.他の分子から酸素を除去したり,水素や電子を与えたりする能力を持つ,つまり還元する能力をもつ分子のことを還元剤といいます.
Fe2O3 + 3CO → 2Fe + 3CO2
ここではCOが酸化鉄から酸素を取り除く還元剤ですが,COは酸素と結合するので酸化されて二酸化炭素(CO2)になります.私たちは鉄に着目するので,この反応を還元反応と言いますが,還元される酸化鉄があれば,必ず酸化されるCOがなければなりません.ですから上の反応は正しくは酸化還元反応と言います.いずれにせよ製鉄業が大量に炭酸ガスを発生することがわかります.
ここで,「ビタミンCってどんな構造? なぜグルコース(ブドウ糖)に近いの? 他に似たようなものってなに?」のところで出てきたビタミンCの構造を下に示します.ビタミンCは化学名をL-アスコルビン酸といいます.L型の意味は,「ビタミンCのL型,D型ってなに?(近日公開予定)」をご覧ください .L-アスコルビン酸は以前とは違う形,五角形の構造で書きました.炭素に1から6まで番号を付けました.
ビタミンCは体内で多くの分子やイオンを還元することで生命を維持しています.一例として,鉄の3価のイオン,Fe3+を取り上げます.先ほどのFe2O3の鉄もFe3+です.金属の価数は本来の金属が酸化されて失った電子の個数を表します.もちろん失った電子は消えるわけではなく酸素に移ります.
食品中の鉄は空気中の酸素で酸化されてFe3+として存在します.ヒトの小腸には2価イオンを吸収するタンパク質がありますが,3価の鉄イオンは吸収できません.そこでL-アスコルビン酸(還元型ビタミンC)がFe3+に電子を1つ与えてFe2+に変えて鉄を吸収します(「貧血の予防に役立つビタミンC」をご覧ください).Fe3+にマイナス電荷をもつ電子を1つ与えるとFe2+になります.下の式をご覧ください.
L-アスコルビン酸は電子を2個与えることができます.2番と3番の炭素に結合した水酸基(-OH)の水素原子(赤で示します)が2個とれ,そこに含まれる2個の電子が2個のFe3+に与えられFe2+が2個生成します.L-アスコルビン酸は水素を失って,つまり酸化されて酸化型のビタミンCであるL-デヒドロアスコルビン酸になります.デは英語のdeで分離を表わし,ヒドロは水素がhydrogenですので,全体としては水素を失ったアスコルビン酸という意味です.なお水素原子は,水素イオン(H+)と電子が結合したものですので,電子がなくなった水素原子は2個のH+になります.
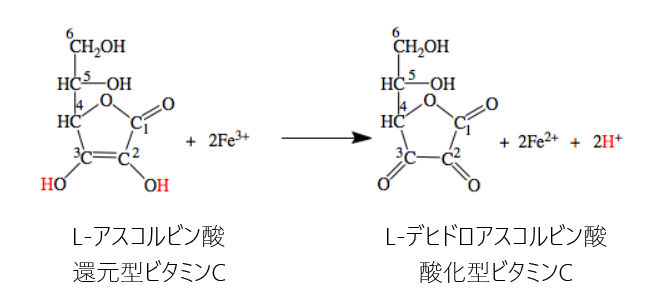
上の反応は,還元型ビタミンCであるL-アスコルビン酸がFe3+を還元してFe2+を生成し,自分は水素を失って(酸化されて)酸化型に変わる酸化還元反応です.
では,酸化型のL-デヒドロアスコルビン酸はどうなるのでしょうか?細胞内では,L-デヒドロアスコルビン酸は酵素によって迅速に還元され,細胞内ではほとんどが還元型のL-アスコルビン酸として存在します.
鉄の吸収以外,L-アスコルビン酸は鉄イオンや銅イオンを還元することで多くの酵素の機能を助けます.ビタミンCを必要とする酵素については,「アドレナリンやオキシトシンの生成におけるビタミンCの役割とは?」を,コラーゲンの成熟については,「血管,皮膚,筋肉はなぜ硬くてしっかりしているの? ―コラーゲン合成とビタミンCの関係―」を,コレステロール代謝については,「なぜビタミンCは,コレステロール値をコントロールするの?」を,抗酸化剤としての機能については,「体の錆の原因である活性酸素種をしっかり取り去るビタミンC」「発がん性のあるニトロソアミンの生成を抑えるビタミンC」などをご覧ください.
[小城 勝相]
